【國家藥監局已批準44個新冠病毒抗原檢測試劑】人民網北京12月22日電 (記者孫紅麗)據國家藥監局官網消息,12月22日,經國家藥監局審查,批準艾維可生物科技有限公司和邁克生物股份有限公司的2個新冠病毒抗原檢測試劑產品。截至目前,國家藥監局已批準44個新冠病毒抗原檢測試劑產品。
國家藥監局表示,藥品監督管理部門將加強相關產品上市后監管,保護患者用械安全。
資料顯示,根據疫情防控工作需要,為進一步保障新冠疫情防控用抗原檢測試劑供應,國家藥監局于12月8日發布《關于延長新冠病毒抗原檢測試劑注冊證有效期的公告》,將已獲準注冊的新冠病毒抗原檢測試劑的注冊證有效期,在原有效期基礎上延長6個月,切實保障相關產品市場供應。
另外,12月9日,經國家藥監局審查,批準佰奧達生物科技(武漢)股份有限公司、基蛋生物科技股份有限公司和泰普生物科學(中國)有限公司3個企業的3個新冠病毒抗原檢測試劑產品。
12月11日,經國家藥監局審查,批準中山生物工程有限公司的新冠病毒抗原檢測試劑產品。
12月12日,經國家藥監局審查,批準鄭州安圖生物工程股份有限公司和廈門為正生物科技股份有限公司的2個新冠病毒抗原檢測試劑產品。
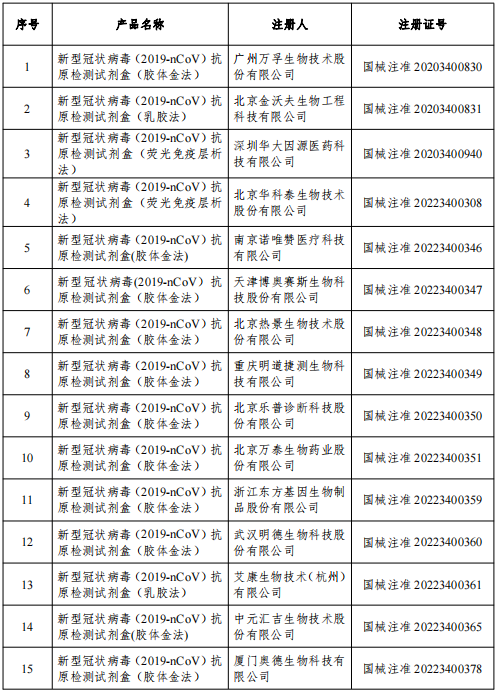
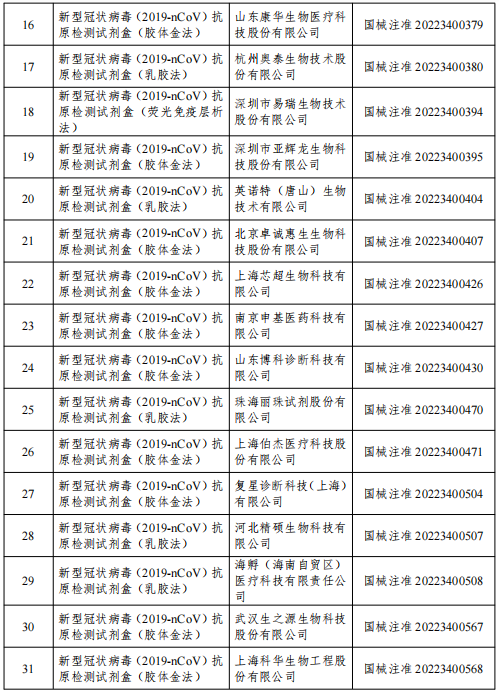
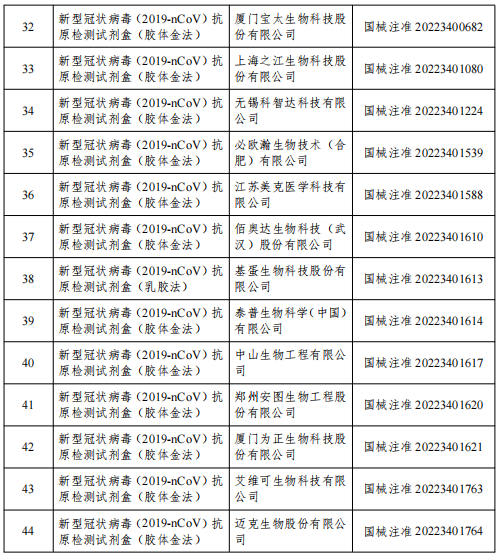
圖表來源:國家藥監局官網
